Домашня Контрольна Робота 2.5
на вівторок 7.03.2017 р.
Здати до першого уроку!!!
5.2.5; 5.3.14; 5.4.13; 5.4.15; 5.5.15; 5.5.26;
5.5.31; 5.6.6; 5.6.11; 5.6.20; 5.6.21; 5.6.25.
Бажаю успіху!
Ефекту "конденсатного одягу"
|
Адіабатичний процес – це процес, який проходить без теплообміну з навколишнім середовищем. У природі такі процеси зустрічаються досить часто. Процес стиснення-розрідження повітря при проходженні звукової хвилі, процеси перемішування великих повітряних мас а також процеси нагрівання та запалення робочої суміші у дизельних двигунах внутрішнього згорання – це далеко не повний перелік реальних процесів, які описуються рівнянням Пуассона.
 |
| Адіабатична хмарка за літаком |
Термодинаміка – це розділ фізики, в якому з найбільш загальних позицій (без розгляду молекулярних уявлень про будову речовини) розглядаються процеси обміну енергії між об’єктом, який вивчається та оточуючим його середовищем.
У всіх процесах, які проходять в природі, енергія не зникає безслідно і не створюється з нічого, а переходить від одного тіла до іншого і перетворюється з одного виду в інший в еквівалентних кількостях.
1. Форвакуумні насоси
1.1 Ротаційний вакуумний насос2. Насоси високого вакууму
1.2 Поршньовий повітряний насос
1.3 Адсорбційний вакуумний насос
1.4 Водоструминний вакуумний насос.
2.1 Насос Ленгмюра3. Вимірювання високого вакууму
2.2 Гетерні комбіновані насоси.
3.1 Манометр Мак-Леода
3.2 Іонізаційний манометр
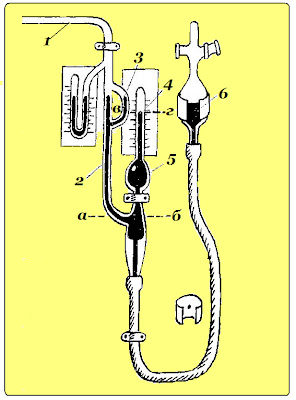 |
| Манометр Мак-Леода |
Теплопровідність – це прцес вирівнювання температур, зумовлений міграцією молекул газу.
Кількість теплоти Q, яка переходить за одиницю часу через одиницю площі поверхні, перпендикулярної до напряму перенесення, прямо пропорційна градієнту температури.
Знак мінус відображає той факт, що теплота йде у напрямку зниження температури.
Коефіцієнт пропорційності χ називають коефіцієнтом теплопровідності. З газів найбільшу теплопровідність має водень, вона у декілька разів перевищує теплопровідність інших газів.
Внутрішнє тертя – це явище виникнення сил тертя між шарами одного газу або рідини, котрі рухаються один відносно другого паралельно з різними швидкостями.
Коефіцієнт внутрішнього тертя (в’язкості) η чисельно дорівнює силі внутрішнього тертя, що діє на одиницю площі, якщо градієнт швидкості шарів дорівнює одиниці. Його вимірюють у кг/м•с або у Па•с.

Остання формула є законом Фіка:N = -D(Δn/Δz)
 |
| Траекторія руху однієї частинки |
1) відсутня взаємодія між молекулами;2) молекули – матеріальні точки певної маси (займають безмежно малий об’єм в порівнянні з об’ємом посудини);3) при зіткненні між собою та зі стінками посудини ведуть себе як пружні кульки;4) молекули рівномірно розподілені по об’єму).